Des tests de diagnostic rapide antigéniques du SARS-CoV-2 (TROD-SC-2) sont maintenant disponibles et accessibles chez les médecins, pharmaciens et infirmières.
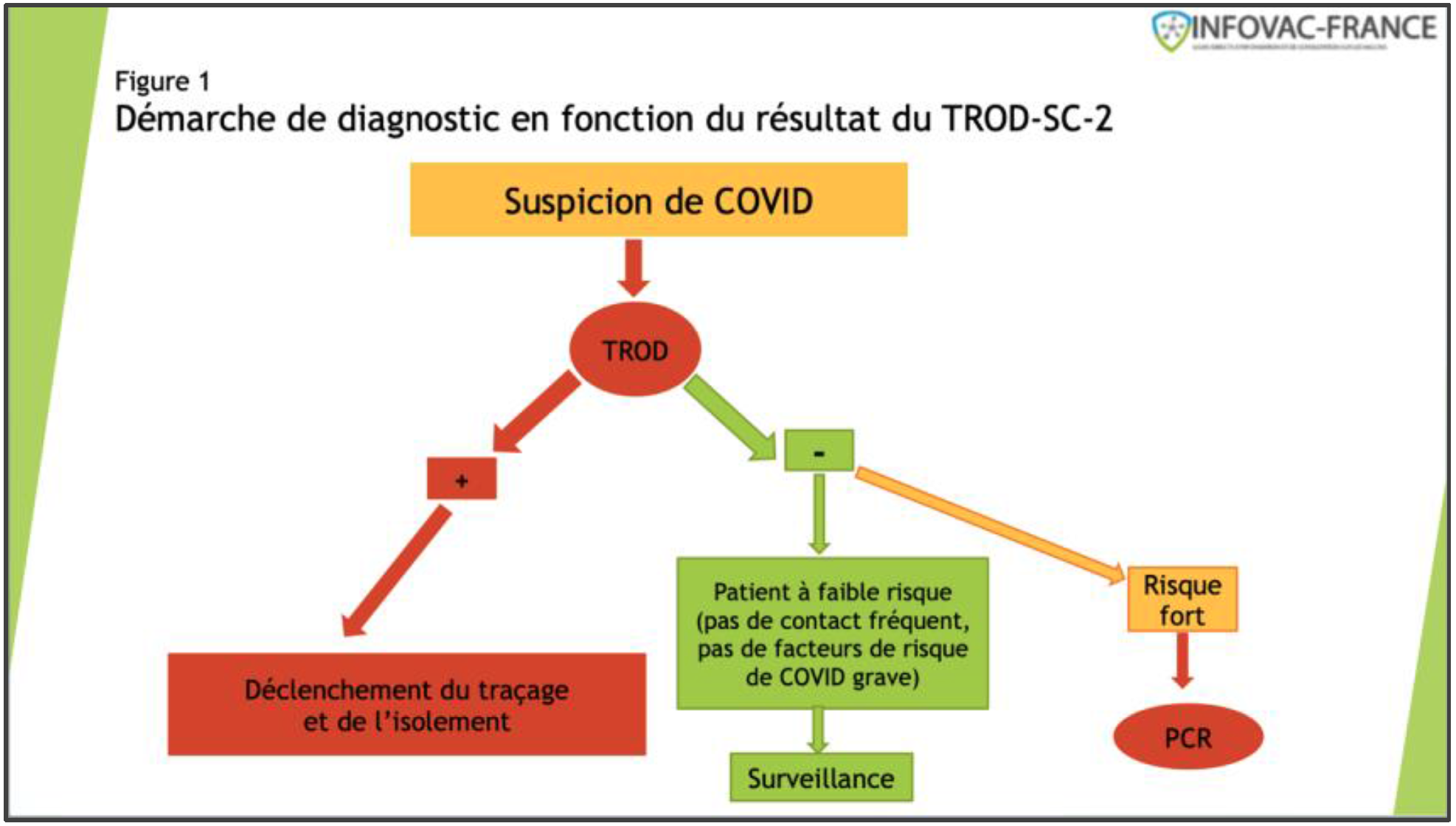
Ils vont même pouvoir justifier d’une cotation relativement avantageuse pour les soignants (2 C pour les médecins). Depuis maintenant plusieurs mois, des articles plaidant pour leur utilisation ont été publiés dans des journaux prestigieux comme le New England Journal of Medicine ou le New York Time, leurs auteurs considérant qu’ils pourraient constituer un tournant dans l’évolution de la pandémie, presque au même titre que les vaccins (1,2,3). Nous même, sur le site InfoVac, nous insistions dès le mois d’Août sur l’importance du développement et de l’utilisation de ces tests, en proposant un algorithme, sans grand succès (Figure 1). Plusieurs mois après, le 6 Octobre 2020, la HAS prend (enfin !) position pour leur mise en pratique dans les premiers jours de symptômes de la COVID-19 (4).
Les TROD-SC-2 sont basés sur la même technologie que celle utilisée depuis 40 ans pour les tests de diagnostic rapide de grossesse, d’angine ou de grippe, les antigènes ciblés étant ceux spécifiques du SARS-CoV-2. Ils ne nécessitent aucune installation particulière, sont extrêmement simples à réaliser et donnent des résultats en quelques minutes. Enfin, le coût des réactifs est 4 fois inférieur à celui des RT-PCR.
Figure 1
En pratique clinique, après la préparation initiale et le prélèvement naso-pharyngé (geste très simple à réaliser en moins de 2 minutes), le test se positive très rapidement, en moins de 5 minutes (le plus souvent moins de 2 minutes !) pour l’immense majorité des patients. En cas de test négatif au bout de 5 minutes, il faut cependant attendre la 15ème minute pour affirmer la négativité, ce qui n’empêche pas de terminer la consultation et de demander au patient d’attendre le résultat soit à l’extérieur du cabinet, soit seul dans une salle d’attente dédiée et ce, toujours en respectant scrupuleusement les gestes barrières.
Les premiers tests disponibles, dès le mois d’Avril 2020, ont démontré leur spécificité (un test positif affirmant l’infection de façon quasi certaine) mais une sensibilité inférieure à celle des RT-PCR. Les TROD-SC-2
actuels sont tout aussi spécifiques et plus sensibles que les premiers, mais restent néanmoins moins sensibles qu’une RT-PCR (5,6).
La quantité d’antigènes viraux est l’élément essentiel de sensibilité des TROD-SC-2. Cette quantité est dépendante du stade de la maladie (Figure 2) et de la qualité du prélèvement.
Figure 2. Chronologie de l’infection à SARS-CoV-2 et de ses examens
Ainsi pour des charges virales élevées, la sensibilité avoisine les 100% mais chute rapidement pour les charges virales plus basses (traduites par un nombre de cycles en RT-PCR > 30) (7,8).
Or, la charge virale est très élevée dès le début des symptômes mais diminue rapidement après le 4ème jour.
La qualité du prélèvement est essentielle et représente le point délicat de la technique, car les résultats, en terme de sensibilité (possibilité de faux négatif), dépend quasi-exclusivement de la quantité de virus présents. (Vignettes 1, 7,8). La quantité de virus étant moins importante dans la salive, la majorité des études ont été réalisées à partir de prélèvements naso-pharyngés.
Ceci diffère des RT-PCR qui amplifient les gènes viraux recherchés. Un prélèvement de qualité médiocre ou moyenne par RT-PCR se traduit par un nombre plus important de cycles nécessaires pour détecter la présence de virus, mais par un résultat qui passe de la zone positive à négative pour un TROD-SC-2.
Aujourd’hui la HAS propose que ces tests soient uniquement utilisés chez les sujets symptomatiques, lors des quatre premiers jours de symptômes (charge virale élevée), et qu’ils soient réalisés par un professionnel de santé (4).
Très récemment, l’Assurance Maladie a posé des conditions très restrictives pour la réalisation de ces tests chez un patient symptomatique :
- Une RT-PCR n’est pas possible sous 48H
- Le patient a moins de 65 ans et sans facteur de risque (FDR)
- Le test est réalisé moins de 4 jours après le début des symptômes
Les deux premières restrictions semblent contre-productives et responsables d’une perte de temps dommageable. En effet, si le patient est symptomatique, quel que soit son âge ou ses FDR, un résultat positif est une information essentielle à obtenir immédiatement, car la spécificité proche de 100% affirme sans ambiguïté le diagnostic de maladie à SARS-CoV-2. Dans le cas d’un patient à risque, le test RT-PCR sera prescrit en ambulatoire afin d’exclure le diagnostic (Figure 1). Ces TROD-SC-2 doivent permettre ainsi de désengorger les laboratoires d’analyses et d’obtenir des résultats de RT-PCR dans un délai court (24-48H). Par ailleurs, comment s’assurer de la réalisation d’un test RT-PCR dans les 48 heures ? Qui doit rechercher ce RDV ? Le médecin en consultation ? Le patient ? … Doit-on adresser nos malades dans des centres de prélèvements sans RDV et les faire attendre plusieurs heures à l’extérieur ?
Les médecins de soins primaires ont été confrontés à ces situations ces dernières semaines, et forts de leur expérience cauchemardesque pour orienter leurs patients afin d’obtenir des RT-PCR rapidement, ils peuvent affirmer que ces deux critères d’exclusion à la réalisation d’un TROD-SC-2 ne sont pas pertinents et surtout source de réelles difficultés lors de la consultation d’un patient symptomatique.
Outre leur intérêt incontestable pour une personne symptomatique ou ayant un contact connu, de nouvelles indications de ces TROD-SC-2 devraient rapidement voir le jour. En effet, il existe une relation entre charge virale et risque de transmission : plus la charge virale d’un patient est élevée (donc TROD-SC-2 positif), plus il est contagieux. Il est donc logique de penser que le patient dont le TROD-SC-2 est négatif (charge virale faible) n’est pas ou peu contagieux. Ainsi ces tests pourraient être réalisés avant l’entrée dans un lieu où le port du masque permanent est difficilement applicable : restaurants, fêtes familiales, voyages en avion, etc…
De même, dans de nombreux hôpitaux, tous les patients admis en hospitalisation subissent une RT-PCR et sont considérés comme potentiellement infectés en attendant les résultats. La réalisation d’un TROD-SC-2 pourrait faciliter l’orientation précoce des malades.
Ceci gommerait un des défauts des RT-PCR qui restent bien plus longtemps positives alors même que les sujets ne sont plus contagieux (9).
Il est donc urgent de ne plus perdre de temps et de mettre ces TROD-SC-2 à disposition des médecins, infirmiers et pharmaciens, en modifiant leurs conditions de réalisation.
Vignette clinique
Mme B. vient consulter car elle a de la fièvre depuis 3- 4 jours, est enrhumée et a mal à la gorge. Elle est accompagnée de l’un de ses enfants, adolescent, qui présente, depuis une huitaine de jours, des signes respiratoires et se plaint de moins bien percevoir les odeurs et le goût des aliments.
En cette période de circulation du SARS-CoV-2, je propose un test de diagnostic rapide (TROD-SC-2) à la mère qui semble être en début de maladie et une PCR à son fils car il présente des symptômes depuis plus de 8 jours.
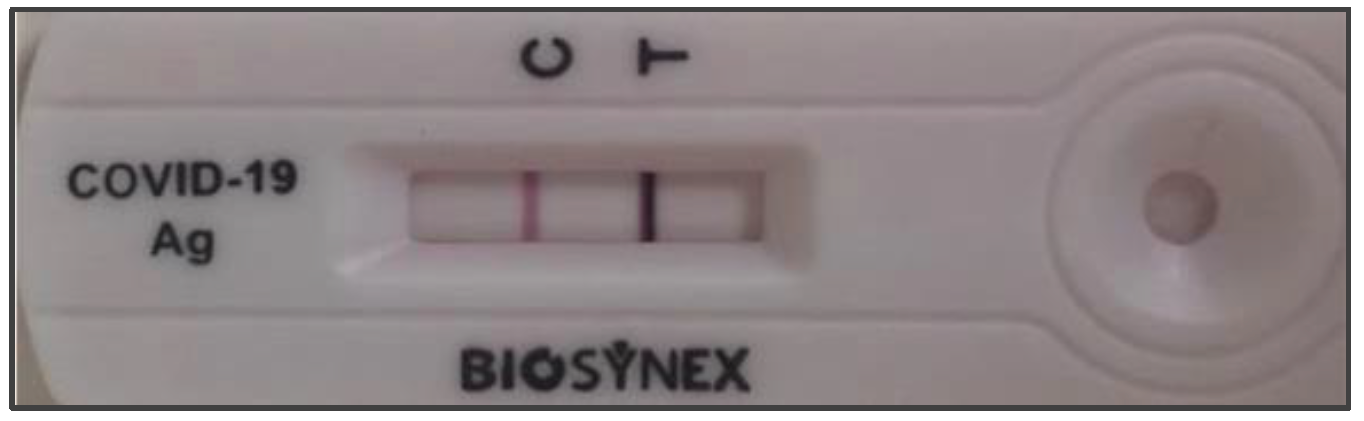
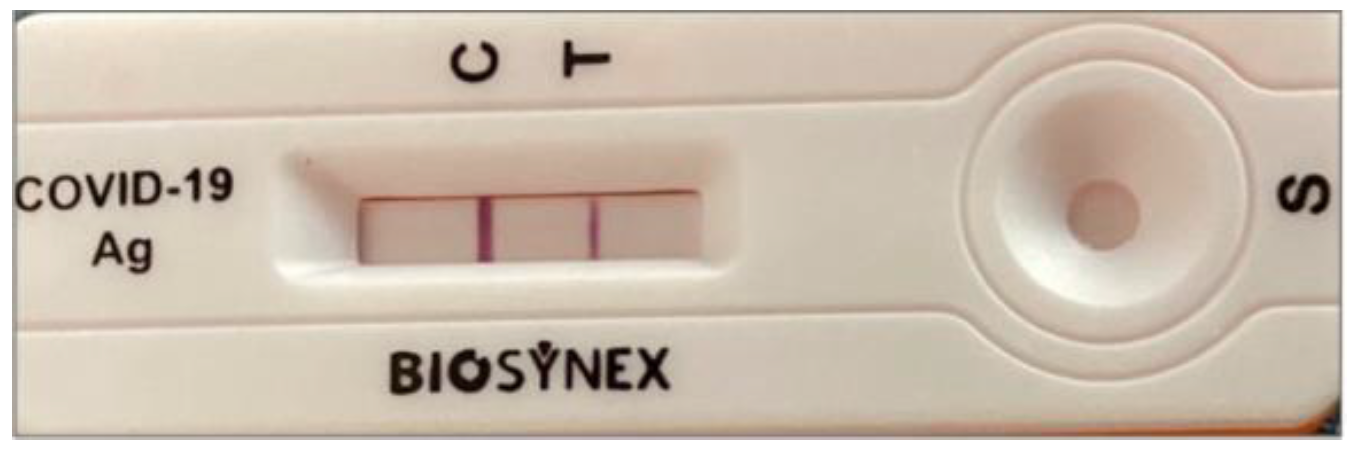
Le TROD-SC-2 de la mère se positive en moins d’une minute (photo 1).
|
|
Photo 1 TROD-SC-2 de la mère C : trait contrôle T : trait de positivité bien plus foncé que le trait contrôle |
En attendant le résultat de la PCR du fils (obtention en 20 minutes sur la machine utilisée) j’explique, à la mère, les mesures à prendre : isolement, durée de l’arrêt de travail, et information de toutes les personnes avec lesquelles elle a été en contact cette dernière semaine.
Au bout de 20 minutes, le résultat de PCR de l’adolescent apparaît sur la machine comme « invalide ».
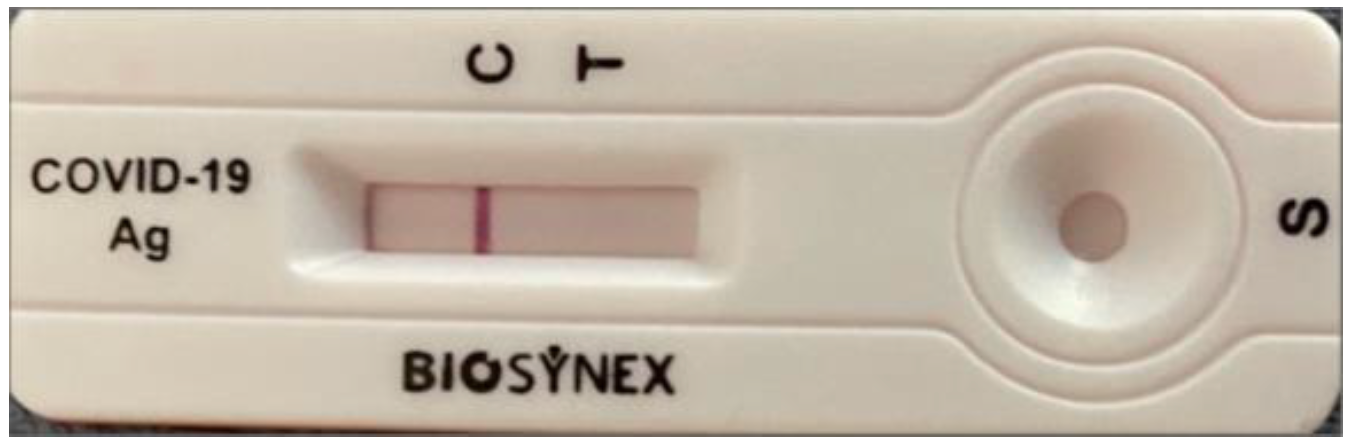
Je décide donc d’une part, de lui faire un test de diagnostic rapide qui va s’avérer faiblement positif en 15 minutes (Photo 2)
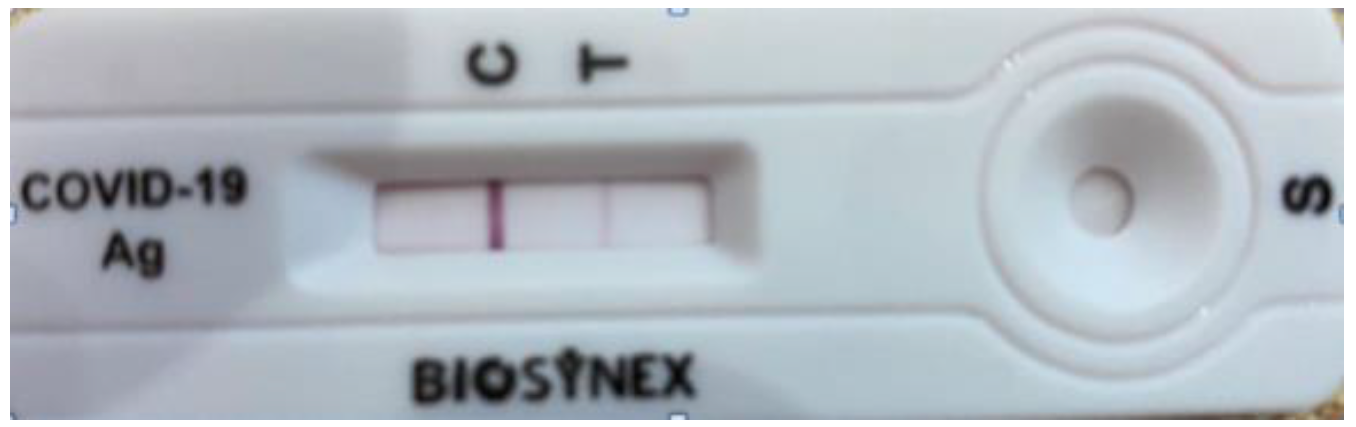 |
Photo 2 TROD-SC-2 de l’adolescent C : trait contrôle T : trait de positivité bien plus clair que le trait contrôle |
et d’autre part, de réaliser une nouvelle PCR avec le reste du liquide (aliquote) de la première.
Cette seconde PCR sera positive avec un nombre de cycles supérieur à 30 pour les 2 antigènes testés, témoignant d’une charge virale peu élevée (photo 3).
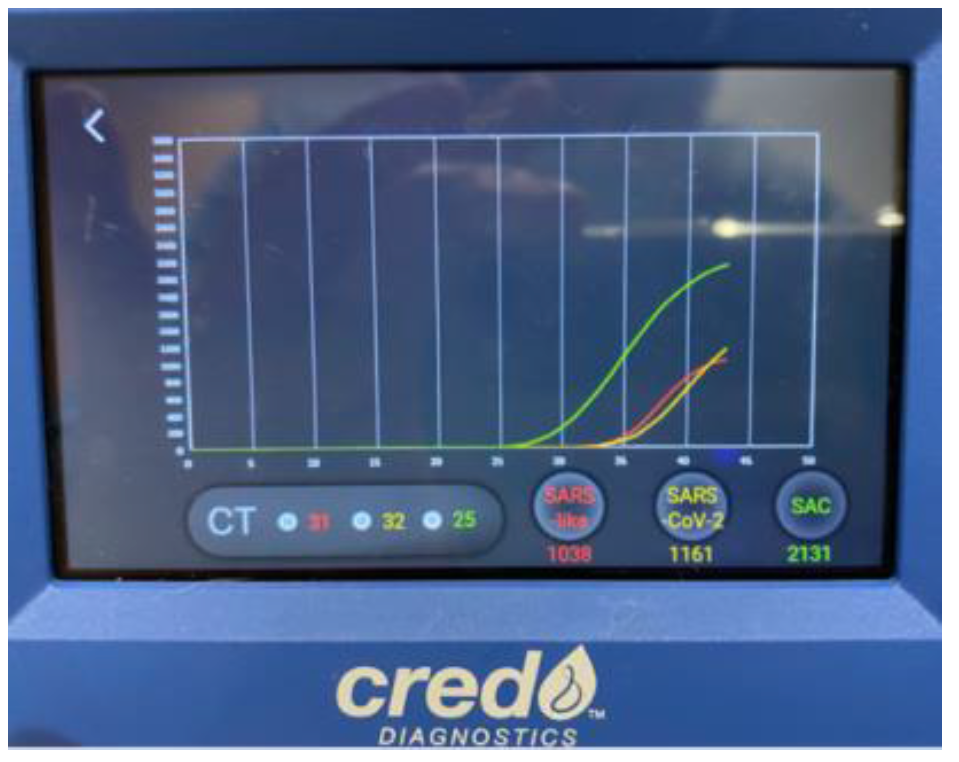 |
Photo 3 Résultat de la seconde PCR de l’adolescent réalisée sur l’aliquote de la 1ère PCR Courbe verte : amplification du gène contrôle présent sur les muqueuses respiratoires Courbes rouge et jaune : amplification de gènes du SARS-CoV-2 |
Je réalise ensuite deux TROD-SC-2 avec le liquide restant de la première PCR (l’aliquote) : il sera négatif en utilisant 20µl, et positif avec 200 µl (photo 4).
|
Photo 4 Test négatif avec 20 µlitres d’aliquote |
Test positif avec 200 µlitres d’aliquote |
Commentaires :
Le Test de Diagnostic Rapide a une excellente sensibilité dans les premiers jours de la maladie, comme en témoigne la positivité rapide du test réalisé chez la mère, mais moins bonne lorsque la quantité de virus diminue. Une positivation rapide du test et un trait intense plaident pour une charge virale élevée.
La négativité du TROD quand la quantité de liquide provenant de l’aliquote est faible et sa positivité quand elle est plus importante confirment à la fois que la sensibilité de ces tests est très dépendante de la quantité d’antigènes et que l’évaluation des TROD sur des aliquotes, telle qu’elle a été réalisée à l’AP ou dans d’autres structures, la sous-estime.
Ceci doit faire relativiser les évaluations faites dans les différents hôpitaux à partir des aliquotes de RT-PCR concluant à des sensibilités non optimales, les résultats étant dépendants de la quantité d’antigènes, elle-même liée au volume d’aliquote utilisé.
Ces TROD-SC-2 sont donc probablement plus sensibles, même avec des charges virales un peu plus faibles, qu’il ne l’a été suggéré jusqu’à présent.
Robert COHEN, Robert TOUITOU, Corinne LEVY
Bibliographie
- Wu KJ. ‘It’s Kitchen Sink Time’: Fast, Less-Accurate Coronavirus Tests May Be Good Enough.New York Time August 6 2020
- Tromberg B, Schwetz T, Perez‑Stable E et al Rapid Scaling Up of Covid-19 Diagnostic Testing in the United States — The NIH RADx Initiative. New England J Med 2020 September 10 DOI: 1056/NEJMsr2022263
- Mina M, Parker R, Larremore New England J Med September 30 DOI: 10.1056/NEJMp2025631
- https://www.has-sante.fr/upload/docs/application/pdf/2020-10/synthese_tests_antigeniques_vd.pdf
- Kontou PI, Braliou GG, Dimou NL, Nikolopoulos G, Bagos PG. Antibody Tests in Detecting SARS-CoV-2 Infection: A Meta-Analysis. Diagnostics (Basel, Switzerland) 2020;10(5). http://dx.doi.org/10.3390/diagnostics10050319
- Deeks JJ, Dinnes J, Takwoingi Y, Davenport C, Leeflang MMG, Spijker R, et al. Diagnosis of SARS-CoV-2 infection and COVID-19: accuracy of signs and symptoms; molecular, antigen, and antibody tests; and routine laboratory markers [Protocol]. Cochrane Database of Systematic Reviews 2020;4(CD013596). http://dx.doi.org/10.1002/14651858.CD013596
- FOURATI S, AUDUREAU E, CHEVALIEZ S, PAWLOTSKY JM.Évaluation de la performance diagnostique des tests rapides d’orientation diagnostique antigéniques SARS-CoV-2. Evaluation APHP Septembre 2020
- Fafi-Kremer S et al. Evaluation du test antigénique Biosysex®. Institit virologique de Strasbourg
- Tom M, Mina M. To Interpret the SARS-CoV-2 Test, Consider the Cycle Threshold Value. Clinical Infectious Diseases, ciaa619, https://doi.org/10.1093/cid/ciaa619