Pourquoi et comment le booster augmente-t-il la réponse immunitaire ? La vaccination (ou l’infection) entraîne une augmentation du nombre de cellules immunitaires spécifiques à (ou aux) antigène(s) présenté(s). Ces cellules produisent des anticorps et d’autres molécules permettant de lutter contre l’agent pathogène. Ce pool de cellules immunitaires (plasmocytes à longue demi-vie) diminue ensuite lentement. Parallèlement s’installe une immunité mémoire grâce aux lymphocytes B et T « mémoires », qui nécessite un temps minimum (4 à 6 mois) de maturation et de différenciation pour être pleinement efficaces lors d’infections futures par cet agent pathogène. Cette dose de vaccin administrée plusieurs mois après la première immunisation a plusieurs effets sur ces cellules :
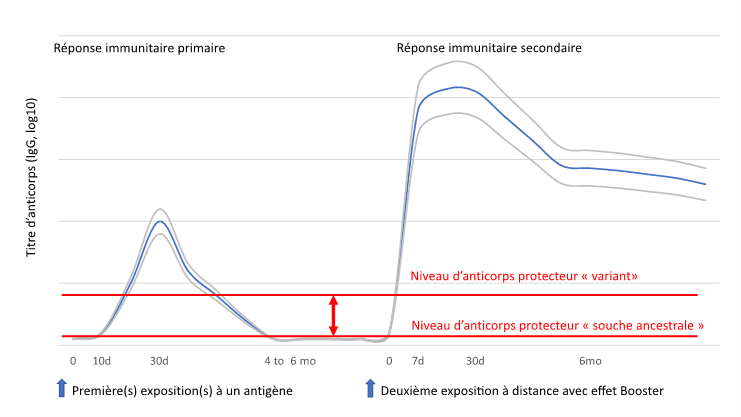
– Il provoque la multiplication des cellules B productrices d’anticorps, ce qui augmente le taux d’anticorps contre l’agent pathogène à des taux supérieurs à ceux obtenus au décours de la primovaccination (Figure 1). Avec le temps, leur nombre diminuera à nouveau mais le pool de cellules B « mémoires » sera plus important, ce qui entraînera une réponse plus rapide et plus forte lors des expositions ultérieures. Ceci est maintenant démontré après la troisième dose de Comirnaty® administré 6 mois après le schéma initial : Les taux d’anticorps sont 5 à 6 fois plus haut qu’après la deuxième dose.
– La diminution du taux des anticorps est plus lente qu’après la primo-vaccination. Une première et courte pente aussi forte qu’après la primo-immunisation et observée puis les titres d’anticorps diminuent beaucoup plus lentement (Figure 1).
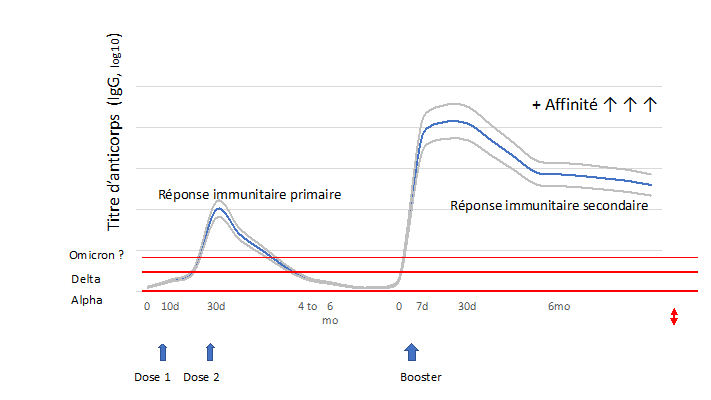
– Il augmente l’affinité des anticorps : les cellules B mémoires migrent vers les ganglions lymphatiques de tout l’organisme où (par leur processus de différenciation et de maturation), elles acquièrent des mutations. Ces mutations produisent entre autres des anticorps qui se lient plus fortement aux agents pathogènes, ce qui peut renforcer leur efficacité.
Pour nombre de vaccins existants, un délai de plusieurs mois (environ 4 à 6 mois) maximise cet effet rappel. Les schémas vaccinaux proposés pour les hexavalents, vaccin anti-pneumococcique conjugué ou contre les papillomavirus suivent ce principe et permettent une immunité de longue durée. Récemment, Pfizer a annoncé qu’une troisième injection du Comirnaty®, administrée 5 à 6 mois après les deux premières doses, suscitait en moyenne des taux d’anticorps trois fois supérieurs à ceux de la deuxième dose, suggérant un effet rappel et laissant entrevoir une bonne efficacité contre le variant ∂. L’efficacité de la dose « booster » réalisée 5 à 6 mois après la primo-vaccination a été évaluée à environ 90% contre le variant ∂ en Israël, tant sur la mortalité que sur les différentes formes de COVID. On peut postuler que la maladie COVID-19, contractée avant ou après une ou deux doses vaccinales, a probablement le même effet de stimulation immunitaire (voire plus) qu’une injection vaccinale. Le nombre de cellules B « mémoires » et les niveaux d’anticorps finissent par se stabiliser après des rappels répétés (ou une réinfection): une injection de rappel suscite des réponses immunitaires plus fortes.
Pourquoi les recommandations d’une dose de « Booster » varient-elles d’un pays à l’autre (âge de recommandation, début du programme) ? Les doses de vaccins étant disponibles, les recommandations dépendent maintenant de la situation épidémiologique, de la date du début du programme de vaccination (les Anglais et les Israéliens ont commencé 3 mois avant nous), de la logistique de la vaccination et des objectifs recherchés :
- si l’objectif est uniquement la prévention des formes graves, il faut proposer un booster aux plus vulnérables, car ce sont eux qui présentent les risques les plus importants. Leur immunité décline plus vite, et ils ont été vaccinés les premiers. L’effet attendu du booster est probablement très prolongé. Les formes graves ne sont pas l’apanage exclusif des plus âgés et une diminution progressive de l’âge (jusqu’à 40 ans ?) pour le booster doit être envisagée. Pour les plus jeunes, une politique acceptable est de les laisser s’immuniser « naturellement » et progressivement par la circulation des variants, étant entendu qu’ils sont très bien protégés contre les formes graves par le schéma de primo-vaccination. C’est le modèle choisi en Angleterre où les mesures de freinage de l’épidémie (distanciation, masques…) ont été stoppées et ou le nombre d’infections a augmenté très rapidement alors que le nombre de décès et des hospitalisations se sont certes accrus mais dans les mêmes proportions. On peut penser que l’attitude qui va être adoptée en France et dans de nombreux pays Européens va y associer un renforcement des mesures de freinages de l’épidémie pour limiter cet hiver la circulation virale et amoindrir le niveau des contaminations.
- si l’objectif est de réduire les infections et la transmission, les sujets plus jeunes doivent être inclus. Il faut noter que cet effet est probablement peu durable, persistant tant que les taux d’anticorps sont suffisamment élevés pour imprégner les muqueuses. Cela peut contribuer à amoindrir un risque épidémique comme en Israël qui a choisi cette option.
- Une patiente de 76 ans vaccinée en avril-mai a fait un COVID léger fin août. Quand lui recommander un rappel ? Elle a eu 3 expositions mais sans un intervalle suffisant avant son infection pour maximiser l’effet « booster ». L’administration d’un rappel 5 à 6 mois après le COVID parait prudent.
- Un patient de 55 ans appartenant à un groupe à risque a fait un COVID en mars 2020 et a eu une dose de vaccin en juin 2021. Quand lui recommander un rappel ? Six mois après sa vaccination, maintenant !